- Szerző Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:41.
- Utoljára módosítva 2025-06-01 07:36.
Fő különbség - alifás és aromás szénhidrogének
Lássuk először röviden, hogy milyen szénhidrogének tárgyalják az alifás és aromás szénhidrogének közötti különbséget. A szénhidrogének olyan szerves vegyületek, amelyek szerkezetükben szén- és hidrogénatomokat tartalmaznak. A legfontosabb különbség az alifás és aromás szénhidrogének között az, hogy az alifás szénhidrogének nem tartalmaznak konjugált kötésrendszert, míg az aromás szénhidrogének konjugált kötésrendszert tartalmaznak. Mindazonáltal mindkét molekula szerves vegyületnek minősül.
Mik azok az alifás szénhidrogének?
Az alifás szénhidrogének azok a szerves molekulák, amelyek szerkezetükben szén (C) és hidrogén (H) atomokat tartalmaznak; egyenes láncokban, elágazó láncokban vagy nem aromás gyűrűkben. Az alifás szénhidrogének három fő csoportba sorolhatók; alkánok, alkének és alkinok.
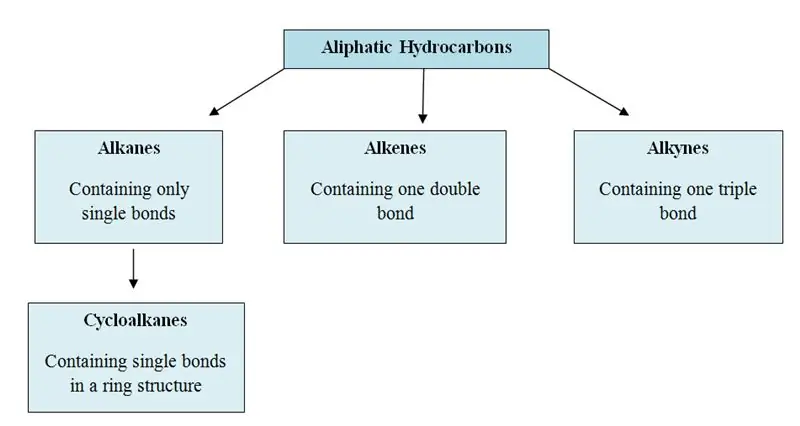
Mik azok az aromás szénhidrogének?
Az aromás szénhidrogéneket néha „aréneknek” vagy „aril-szénhidrogéneknek” is nevezik. A legtöbb aromás szénhidrogén szerkezete benzolgyűrűt tartalmaz; de vannak nem-benzol aromás szénhidrogének, amelyeket heteroaréneknek neveznek, és amelyek a „Huckle-szabályt” követik (a Huckle-szabályt követő ciklikus gyűrűk 4n+2 számú π-elektronnal rendelkeznek; ahol n=0, 1, 2, 3, 4, 5, 6). Egyes aromás szénhidrogéneknek egynél több gyűrűje van; ezeket policiklusos aromás szénhidrogéneknek nevezik.
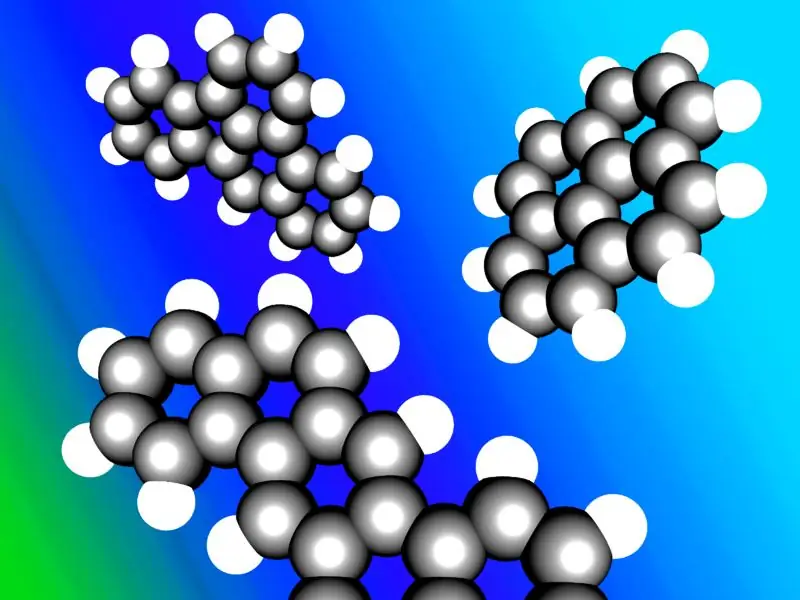
Tipikus policiklusos aromás szénhidrogének illusztrációja.
Mi a különbség az alifás és aromás szénhidrogének között?
Alifás és aromás szénhidrogének szerkezete
Alifás szénhidrogének: Szerkezetükben egyenes láncok, elágazó láncok vagy nem aromás gyűrűk vannak. Ez a csoport telített és telítetlen szénhidrogéneket is tartalmaz. Az alkánok telített szénhidrogének, az alkének és az alkinok telítetlen szénhidrogének.
Egyenes láncok:
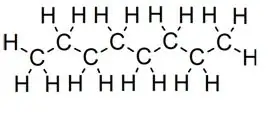
Oktánszám
Márkás láncok:
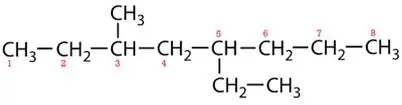
5-etil-3-metiloktán

2-metil-3-pentence
Nem aromás gyűrűk:
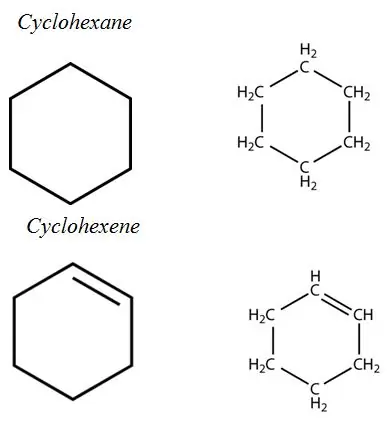
Aromás szénhidrogének: Az aromás szénhidrogének szerkezetében aromás gyűrűrendszer található. Ezek mind telítetlen szénhidrogének, de viszonylag stabilak a konjugált kötésrendszer miatt.
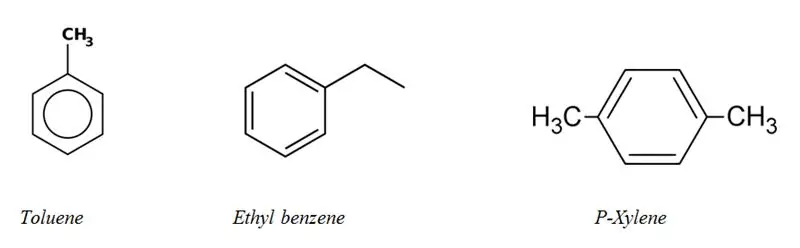
Alifás és aromás szénhidrogének kategóriái
Alifás szénhidrogének:
Az alifás szénhidrogénekben három fő csoport van; alkánok, alkének és alkinok. Allil szénhidrogénekként is ismertek.
Alkánok: Az alkánokban a szén- és hidrogénatomok egyszeres kötéssel kapcsolódnak egymáshoz. Nincs több kötvényük. Az alkánok gyűrűs szerkezeteket alkotnak, ezeket cikloalkánoknak nevezik.
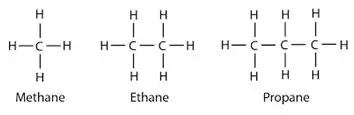
Alkének: Ez a csoport egyszeres és kettős kötéseket is tartalmaz a szénatomok között. A hidrogén- és szénatomok mindig egyes kötéseket alkotnak.
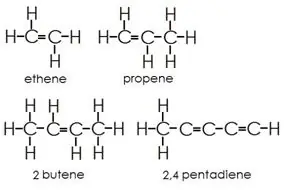
Alkinek: Az alkinek az egyszeres kötéseken kívül hármas kötéseket is tartalmaznak a szénatomok között.
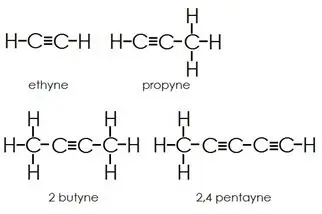
Aromás szénhidrogének:
A legtöbb aromás szénhidrogén szerkezete legalább egy benzolgyűrűt tartalmaz. De kevés a nem benzol aromás szénhidrogén, ezeket „heteroaréneknek” nevezik. Az aromás szénhidrogéneket „aril” szénhidrogéneknek nevezzük.
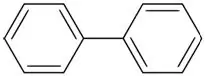
Bifenil (aromás szénhidrogén két benzolgyűrűvel)
Alifás és aromás szénhidrogének kötési mintája
Alifás szénhidrogének:
Alifás szénhidrogénekben; egyszeres, kettős vagy hármas kötések a molekulában bárhol létezhetnek. Néha több szerkezet is létezhet egy molekulaképlethez a többszörös kötés helyzetének megváltoztatásával. Ezeknek a molekuláknak lokalizált elektronrendszerük van.
Aromás szénhidrogének:
Az aromás szénhidrogénekben van egy alternatív egyszeres és kettős kötésrendszerük, amelyek konjugált kötésrendszert alkotnak egyes elektronok delokalizálása érdekében. (A delokalizált elektronok egyik kötésről a másikra mozoghatnak.)
Alifás és aromás szénhidrogének reakciói
Alifás szénhidrogének:
A telített szénhidrogének szubsztitúciós reakciókon mennek keresztül; a telítetlen szénhidrogének addíciós reakcióval érik el a stabilitást. Néhány reakció azonban ellenőrzött körülmények között, többszörös kötés felszakadása nélkül megy végbe.
Aromás szénhidrogének:
Az aromás szénhidrogének telítetlenek, de stabil konjugált elektronrendszerük van, így hajlamosabbak szubsztitúciós reakciókra, nem pedig addíciós reakciókra.
Kép jóvoltából: „Polycyclic Aromatic Hydrocarbons” - Inductiveload - A feltöltő saját munkája, az Accelrys DS Visualizer. (Nyilvános domain) a Commonson keresztül






